لیتیم
یک فلز قلیایی نقرهای-سفید و نرم با عدد اتمی ۳ است. این عنصر در شرایط استاندارد دما و فشار سبک ترین فلز و کم چگالی ترین عنصر جامد است. مانند دیگر فلزهای قلیایی، لیتیم هم بسیار واکنش پذیر و آتشگیر است به همین دلیل بیشتر آن را زیر روغن صنعتی نگاه میدارند. اگر بر روی آن برشی پدید آید، بخش بریده شده دارای جلای فلزی خواهد بود اما به دلیل واکنش پذیری زیاد آن خیلی زود با رطوبت هوا واکنش میدهد، هوا باعث خوردگی آن میشود و به رنگ نقرهای تیره مایل به خاکستری و سپس سیاه در میآید. به دلیل واکنش پذیری بالای لیتیم، هرگز نمی توان آن را به صورت عنصر آزاد در طبیعت پیدا کرد. بلکه همواره در بخشی از یک ترکیب شیمیایی که بیشتر یونی است، پیدا میشود. لیتیم در چندتا از کانیهای پگماتیتی یافت میشود اما از آنجایی که در آب حل میشود، به صورت یون در آب اقیانوسها و به صورت نمک در آبها و رس دیده میشود. در رویکرد تجاری، لیتیم را از برقکافتآمیختهای از لیتیم کلرید و پتاسیم کلرید بدست میآورند.
لیتیم و ترکیبهای آن کاربردهای فراوانی دارند از آن جمله در شیشه و سرامیک پایدار در برابر گرما، آلیاژهای با مقاومت بالا نسبت به وزن که در فضاپیماها کاربرد دارد، باتریهای لیتیم و لیتیم-یون. کاربردهای یاد شده بیش از نیمی از لیتیم تولیدی را از آن خود میکند.
در ظاهر این طور به نظر میرسد که لیتیم هیچ نقشی در زندگی حیوانها و گیاهان ندارد و آنها بدون لیتیم هم میتوانند زنده بمانند، اما در عمل در همهٔ اندامهای زنده می توان زدپای بسیار کم رنگ لیتیم را پیدا کرد. یون لیتیم که در قالب نمکهای گوناگون پیدا میشود بر روی اعصاب انسان اثر میگذارد و میتواند به عنوان دارو در درمان اختلال دوقطبی کمک کند.
ویژگی ها
لیتیوم فلز نایابی نیست. میزان لیتیوم موجود در پوسته زمین برابر با ۰،۰۰۶ درصد است که بنظر کم میآید اما همین اندازه نیز از موجودی فلزات دیگر مانند قلع و جیوه بیشتر میباشد.
تنها فرقی که میان لیتیوم و دیگر فلزها وجود دارد، وضعیت پراکندگی آن بر روی کره زمین است.
نخست آنکه مکانهایی که لیتیوم در آنجا گرد آمدهاست زیاد نیستند. منابع قابل توجه و شناخته شده لیتیوم بر روی زمین شیلی، آرژانتین، تبت، چین، ایالت نوادای آمریکا و بولیوی میباشند.
این در حالیست که منابع بولیوی که معدن شناسان میزان ذخایرش را برابر با ذخایر افغانستان تخمین میزنند، هنوز آغاز به بهره برداری نکردهاست.
کاربرد
لیتیوم یکی از اجزاءمهم در باطریهای قابل شارژ است که در تلفنهای همراه، رایانههای دستی و اتوموبیلهای برقی مورد استفاده قرار میگیرد. . در مجموع میتوان گفت که لیتیوم در آینده بسیار نزدیک محبوب کسانی خواهد شد که قصد ساختن بدنه سبک برای خودرو، هواپیما و کپسولهای فضایی را دارند.
آلیاژی از لیتیوم و آلومینیوم هم اکنون در صنایع هواپیما سازی بکار گرفته میشود که سبک، قابل انعطاف و همزمان محکم و مقاوم است.
لیتیوم نیروی کششی زیادی دارد، بخاطر کمی وزن خود گزینه بسیار مناسبی برای باتریهای کم وزن و پرانرژی میباشد.
لیتیوم همراه با سرب آلیاژی را تولید میکند که در ساختن بلبرینگ چرخهای قطار بکار گرفته میشود. لیتیوم حتی در صنایع داروسازی مورد مصرف دارد.
با اینهمه در مورد مصرف لیتیوم هم در صنایع و همچنین در داروسازی توجه به یک نکته بسیار مهم میباشد. مرز میان سودمند بودن این ماده و سمی بودنش برای انسان و محیط زیست بسیار بسیار نازک و شکنندهاست.

یوهان آگوست آرفودسن کاشف لیتیم



 انجام آزمایش: تاثیر سرکه نوشابه و آب بر روی دندان
انجام آزمایش: تاثیر سرکه نوشابه و آب بر روی دندان  عنوان 5
عنوان 5  پی اچ
پی اچ  دموکریت
دموکریت  راکتور هسته ای
راکتور هسته ای 
 معرفی کتاب تست علوم تجربی نهم
معرفی کتاب تست علوم تجربی نهم انتشارکتاب آزمایش های جذاب وکاربردی علوم تجربی هفتم -هشتم ونهم
انتشارکتاب آزمایش های جذاب وکاربردی علوم تجربی هفتم -هشتم ونهم نقد و تحلیل کتاب جدیدالتالیف پایه نهم
نقد و تحلیل کتاب جدیدالتالیف پایه نهم تقسیم بندی مواد
تقسیم بندی مواد تبدیل دماها انلاین + جدول (کلوین.سلیسیوس.سانتیگراد.فارنهایت)+لینک دانلود مطلب
تبدیل دماها انلاین + جدول (کلوین.سلیسیوس.سانتیگراد.فارنهایت)+لینک دانلود مطلب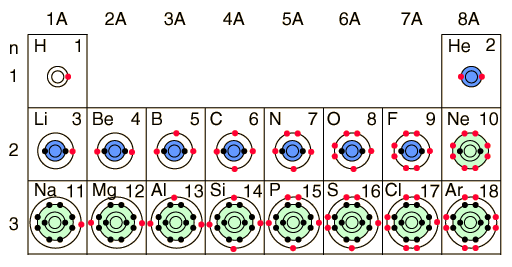 جدول تکمیلی صفحه 7 علوم نهم
جدول تکمیلی صفحه 7 علوم نهم تعریف فیزیک به زبان ساده
تعریف فیزیک به زبان ساده نمونه سوالات علوم دوم راهنمایی+لینک دانلود
نمونه سوالات علوم دوم راهنمایی+لینک دانلود سوالات آزمون علمی آزمایشگاهی دوم راهنمایی 87_88
سوالات آزمون علمی آزمایشگاهی دوم راهنمایی 87_88 اتانول
اتانول مدل های اتمی و ازمایشات دالتون و رادرفورد و بور در مورد اتم ها با جزئیات
مدل های اتمی و ازمایشات دالتون و رادرفورد و بور در مورد اتم ها با جزئیات